“임상 3상 승인을 위해 미 식품의약국(FDA)과 대면 미팅이 예정됐다”. 투자판단을 흐리게 하는 홍보성 내용이나 불리한 항목은 빠뜨리는 제약·바이오 기업의 공시 관행에 제동이 걸린다.
금융위원회와 한국거래소는 9일 공시의 투명성을 높이고 투자 위험을 명확히 파악할 수 있도록 ‘코스닥 제약·바이오 업종 기업의 공시 가이드라인’을 시행한다고 밝혔다. 가이드라인은 투자자가 공시내용을 잘못 판단하도록 유도하거나 이해하기 어려운 제목은 간결하고 쉽게 바꾸도록 했다. 예를 들어 ㄱ사는 난해한 ‘무용성 평가’(약이 치료제로 가치가 있는지를 따져 임상지속 여부를 판단)란 용어를 사용해 임상 시험 결과를 확인했다고 공시했는데, 정작 핵심인 임상시험 중단 권고를 받은 사실은 누락했다. ㄴ사는 임상에 관한 ‘계획’을 승인받았을 뿐인데 임상 승인을 받았다고 공시했다.
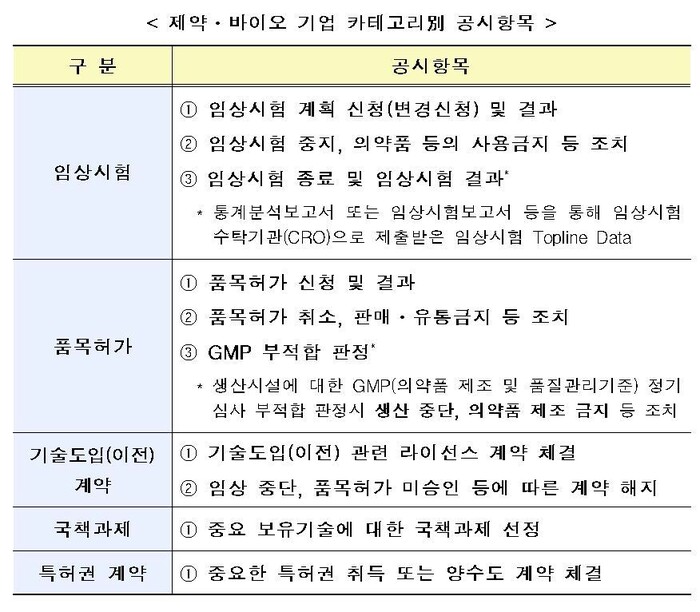
제약·바이오 기업은 기술개발, 임상시험, 품목허가 등 단계별로 불확실성이 높아 주가가 급변한다. 그동안에는 기업이 진행 상황을 자체 판단해 공시해왔는데 충실도가 떨어지거나 투자위험을 알기 어려운 경우가 적지 않았다. 이에 앞으로는 임상시험 중지, 의약품 사용금지 조처, 품목허가 취소, 판매·유통금지 조처 등을 구체적으로 공시해야 한다. 기술도입·이전도 임상 중단·품목허가 미승인 등에 따른 계약 해지 사항 등을 자세히 밝혀야 한다. 이들 공시 사항에 대해서는 모범 공시양식이 제공되고 투자자가 위험성을 파악할 수 있도록 주의문구도 들어간다. 임상시험 공시에 ‘상업화 계획을 변경하거나 포기할 수 있는 가능성도 상존한다'는 문구를 넣는 식이다.
한광덕 선임기자
kdhan@hani.co.kr